
Achivement
研究実績研究実績紹介
-
研究実績
- 論文業績・学会発表
研究実績
-
研究実績
- 論文業績・学会発表
胃癌FOLFOX療法が保険適用されるまで
切除不能胃癌患者さんは経口摂取ができない、肝腎機能障害があるなどの理由でFOLFOX(5-FU/レボホリナート+オキサリプラチン)しか投与できない方がたくさんいます。そこで、「55年通知」を活用して全国でFOLFOXが保険償還されるよう、日本胃癌学会にも働きかけ「医薬品の適応外使用事例」を申請し、2017年2月より保険償還されるようになりました。一方で薬事承認はされないため、FOLFOX+αの治療法開発に影響がでる可能性がありました。そこで「公知申請」を活用するため、「未承認薬・適応外薬の要望」を申請し、2023年3月薬事承認(適応拡大)されました。長い年月がかかりましたが、全国の胃癌患者さんがFOLFOXを使用することが可能になりました。

高度腹水を伴うまたは経口摂取不能の
腹膜転移を有する胃癌に対する化学療法の開発
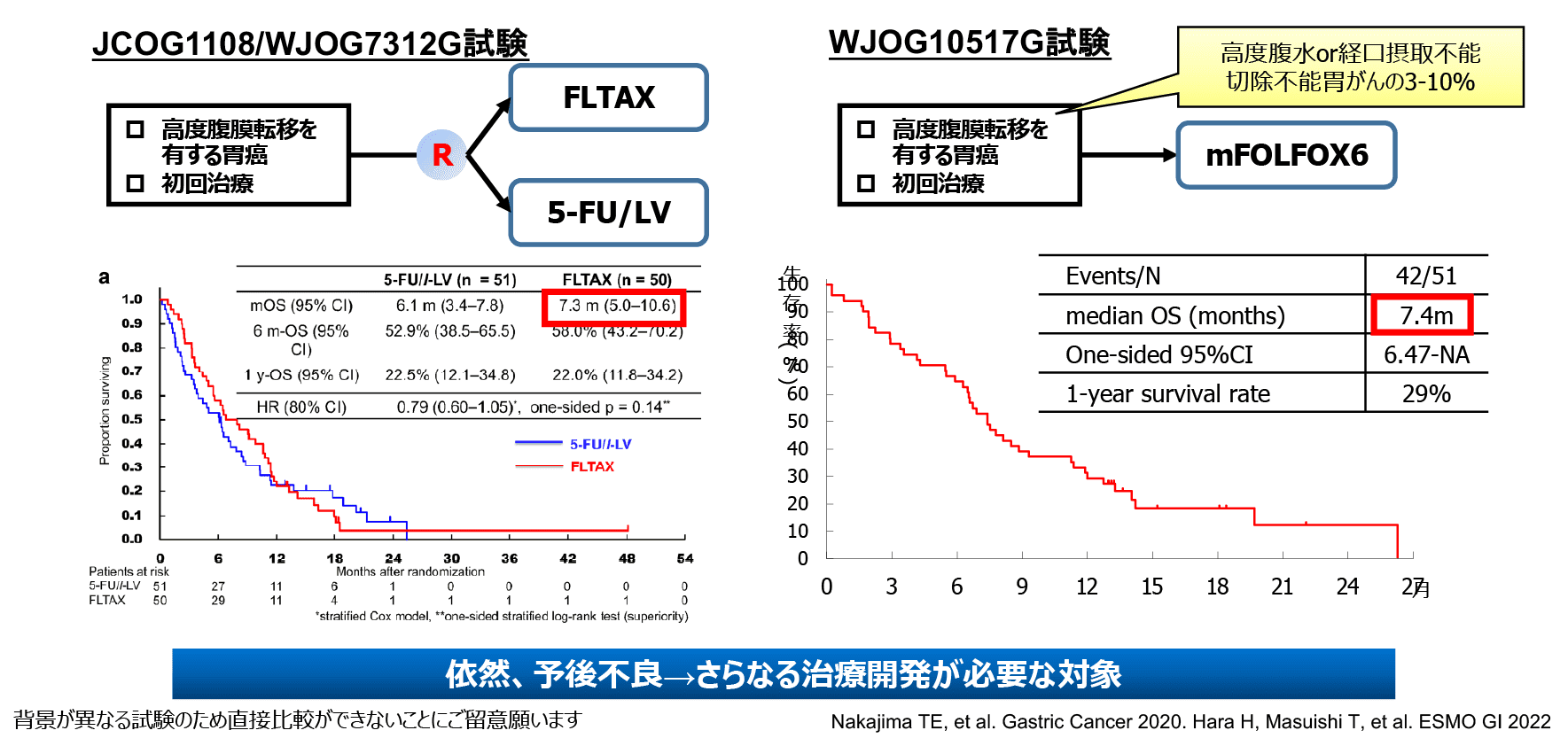
高度腹膜転移胃癌は胃癌全体の3-10%を占め、内服の抗がん剤加療が困難な対象です。当院の後方視的研究などから同対象におけるmFOLFOX6療法の有効性が示唆され、WJOG10517G試験により治療選択肢の1つとなりました。しかしながら、腹水制御割合や経口摂取改善割合などで一定の効果が得られたものの、全生存期間中央値は7か月程度と依然として予後不良な対象です。本邦の胃癌ガイドラインで1次治療における化学療法+ニボルマブ併用療法が推奨される根拠となった第III相試験から同対象は除外されており、ニボルマブ上乗せの有効性と安全性は不明です。そのため同対象におけるmFOLFOX6+ニボルマブ療法の有効性と安全性を探索するWJOG16322G試験を立案し現在進行中です。より有効な治療を患者様に届けられることを期待しています。
高度腹膜転移胃癌に対する治療開発の現状
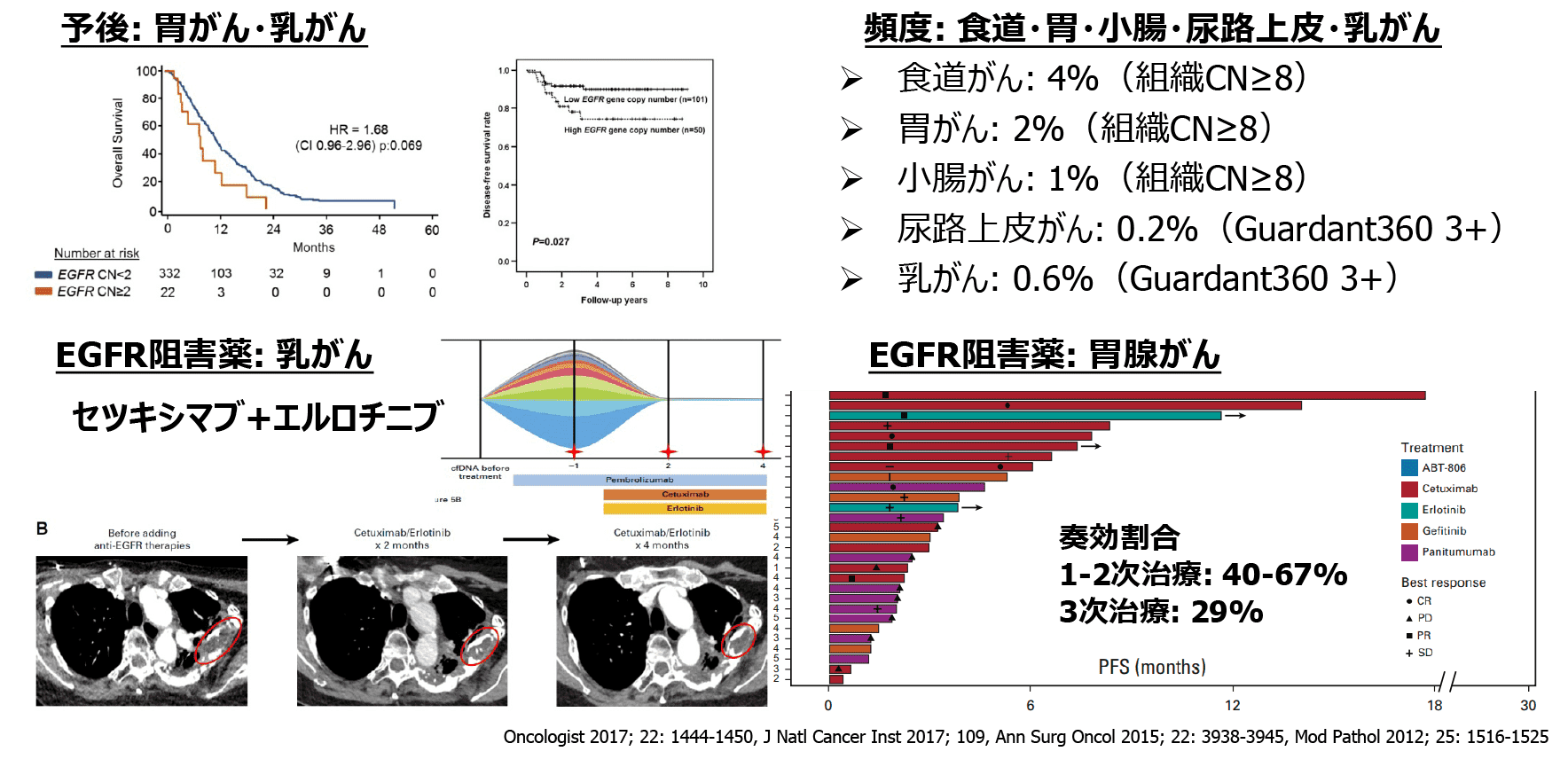
EGFR遺伝子増幅陽性固形癌に対する抗EGFR抗体薬の開発
遺伝子パネル検査を実施しても治療薬に到達できない患者さんがたくさんいる中、1つでも多く治療標的となる遺伝子を見つけ、その遺伝子を標的とした薬剤を承認に結び付けるための研究が必要です。現在、いずれのがん種においてもEGFR遺伝子増幅陽性患者さんに対して薬事承認されている薬剤はありません。本試験により、EGFR遺伝子増幅陽性固形癌患者さんに抗EGFR抗体薬であるネシツムマブが届くことを期待しています。本試験は、先進医療Bとして実施しており、バスケット試験として初の先進医療です。
EGFR増幅陽性固形がん
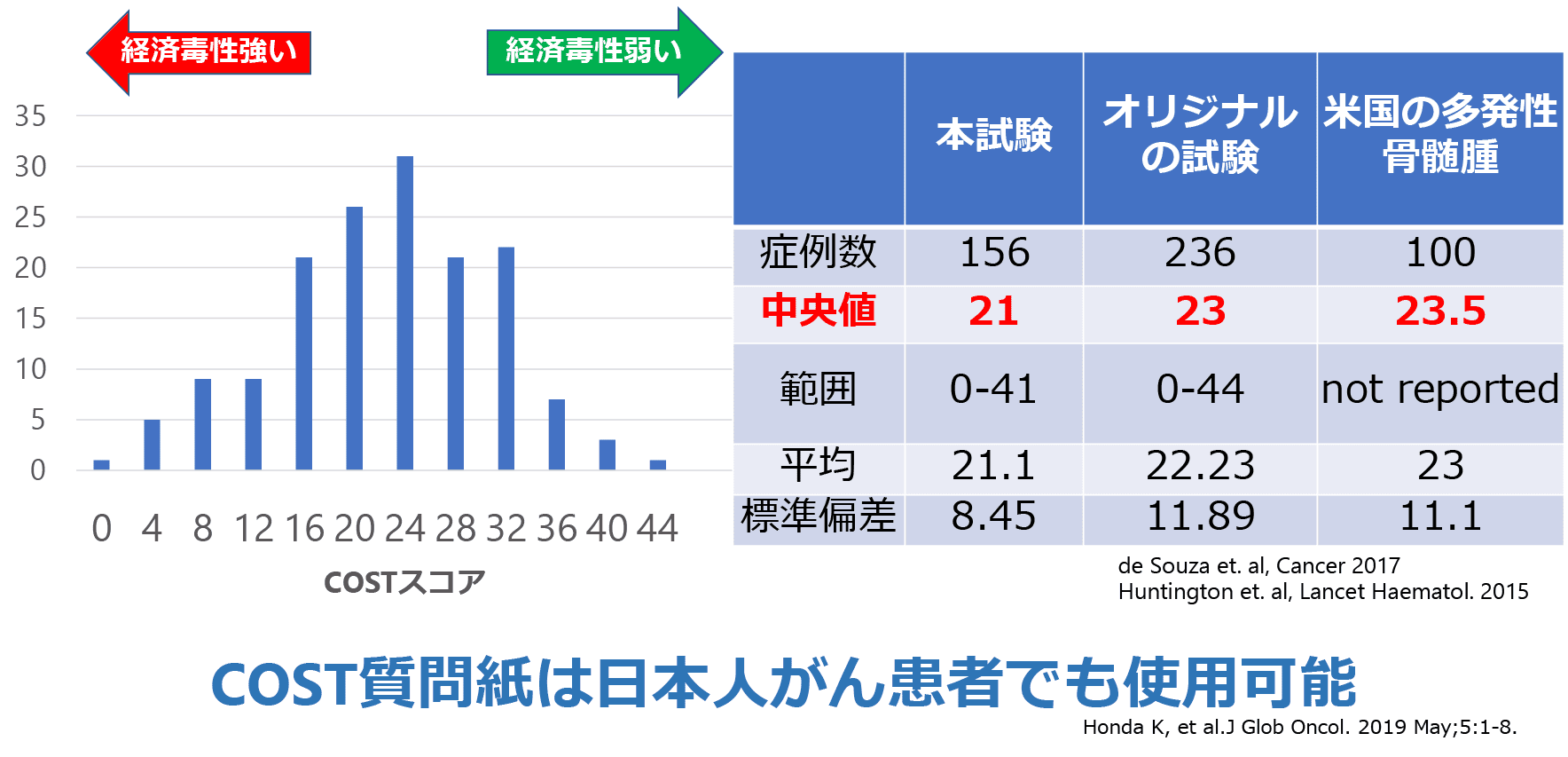
経済毒性
経済毒性はがんに伴う経済的負担が患者・家族に与える苦痛を指します。毎月の治療費などによる出費の増加や長期の治療期間による就労制限などが患者や家族の生活に影響を及ぼします。経済毒性を評価するツールの日本語訳を開発するなど、日本をリードする研究を行っています。
COSTスコア
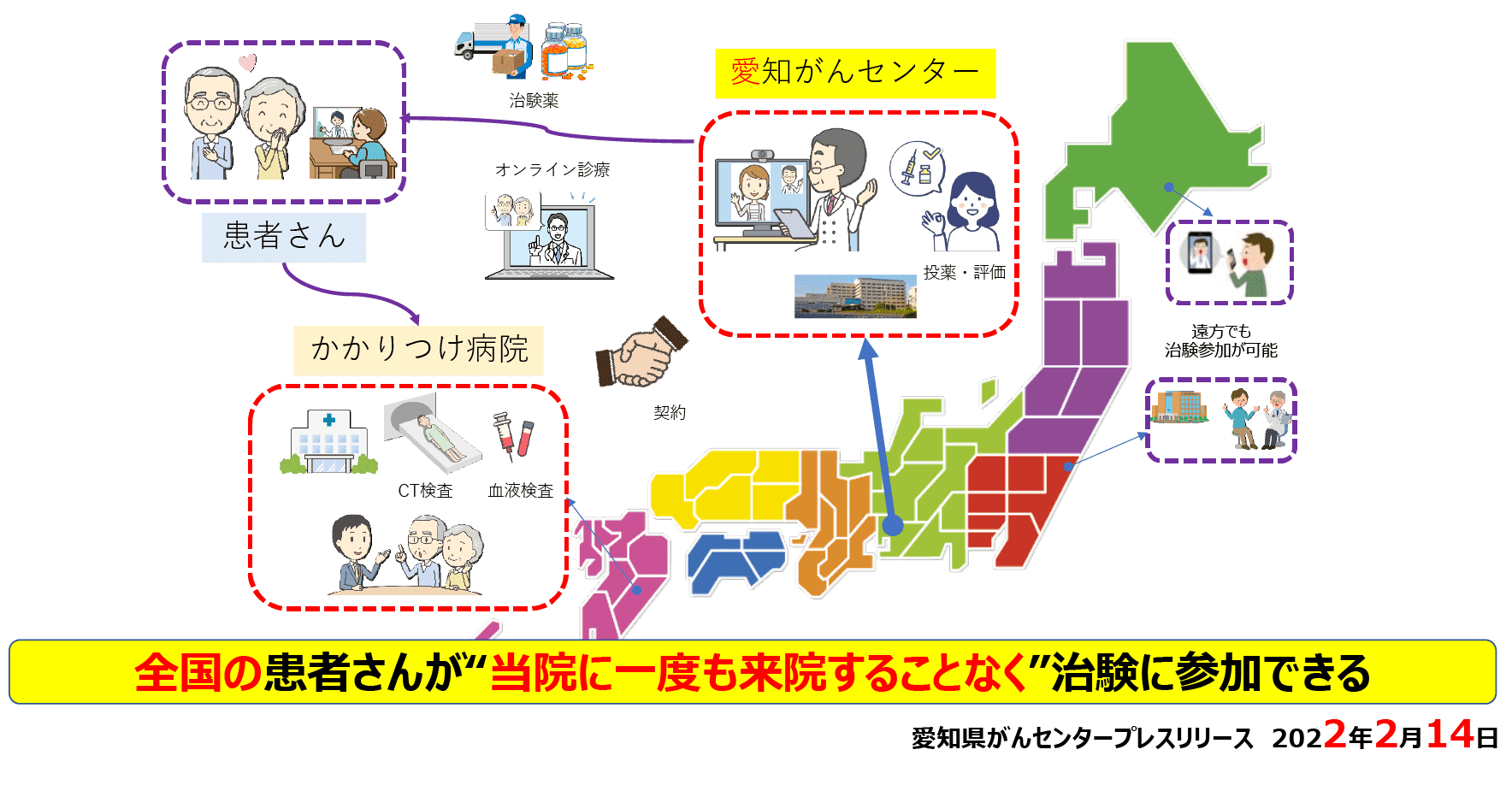
オンライン治験
オンライン治験は、遠方の患者さんが当院に直接来院しなくても治験に参加できるシステムです。2022年には、当科で日本初のオンライン治験が開始され、現在、このような取り組みが全国に広がっています。患者さん、医療従事者、製薬企業、そのほか治療開発に携わる全ての人々にとってメリットのある枠組みを目指しています。

オンライン診療を活用した遠隔治験
ALK融合遺伝子陽性の
進行・再発固形腫瘍に対するALK阻害薬の開発
ALK融合遺伝子陽性の進行・再発の固形腫瘍患者さんを対象にブリグチニブ療法の有効性と安全性を検討する第Ⅱ相バスケット試験(WJOG15221M/ALLBREAK試験)を立案し、現在進行中です。この試験では、より多くの患者さんに試験に参加いただけるようにオンライン治験を導入しています。また、候補の患者さんをより多く同定するため、腫瘍組織を用いたALKの免疫染色によるスクリーニング研究を並行して実施しております。
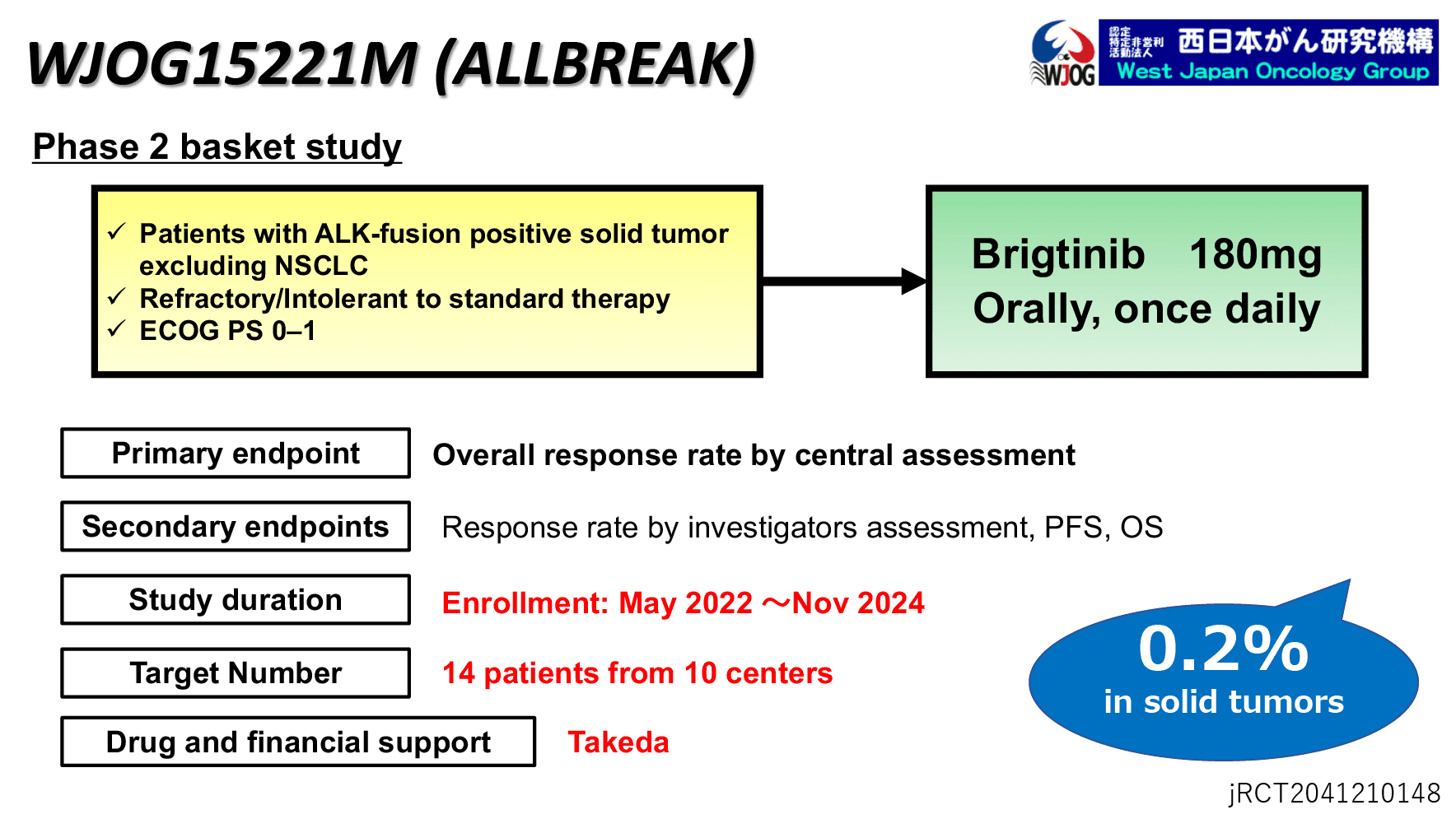
新たな臨床試験(プラグマティック試験)
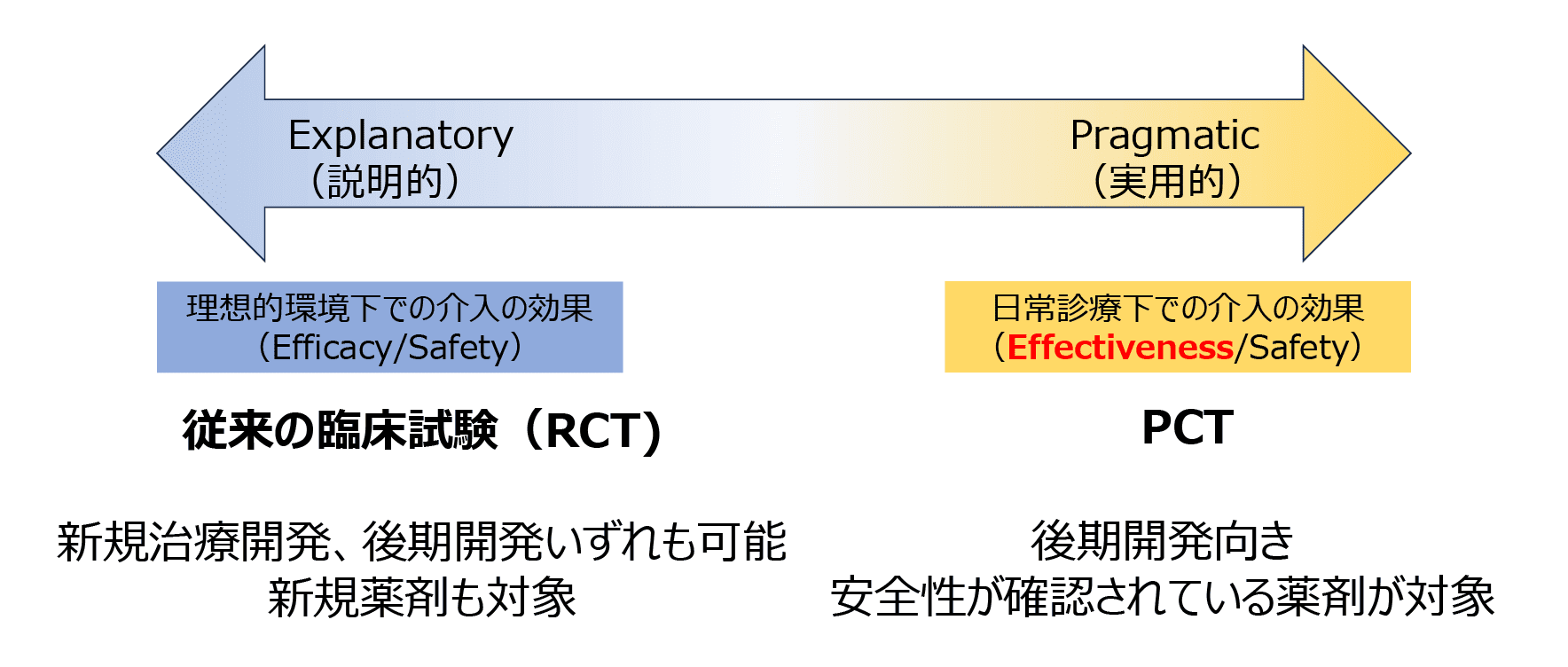
プラグマティック臨床試験とは、日常臨床にできるだけ近い条件で行う試験です。当科は、2023年12月に全国250施設の無償協力のもと、がん領域初のプラグマティック第Ⅲ相試験(PRABITAS試験)を開始しました。効率的な運営により大規模な資金を得ずに第Ⅲ相試験を実現しました。
PCTとRCTの概念図
PanAsia ガイドライン
日本臨床腫瘍学会(JSMO:Japanese Society of Medical Oncology)では、欧州臨床腫瘍学会(ESMO: European Society for Medical Oncology)との協同事業として、Pan-Asian Guidelines Adaptation (PAGA) projectが各癌腫で行われております。当科からは食道癌、胃癌、大腸癌の分野で本事業に参画し、日本からだけではなくグローバルな視点でがん薬物療法に関するガイドラインを議論しています。

消化管癌における
血中Cell-free DNA (cfDNA)に関する研究
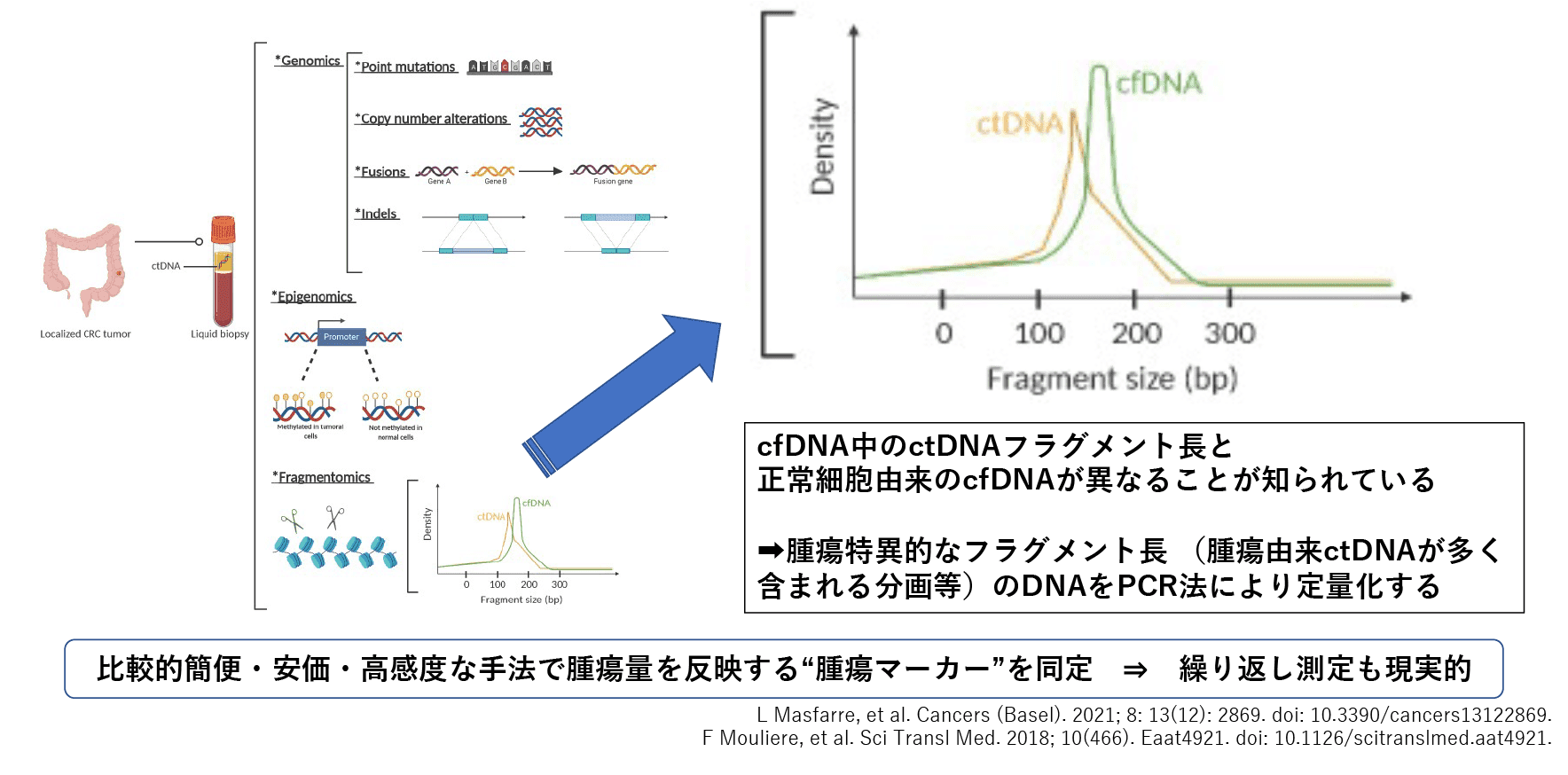
体細胞由来のCell-free DNA(cfDNA)は通常血中を循環していますが、担がん患者様の血中にはがん細胞由来のcfDNAが微量に存在しています。cfDNAの半減期は数時間程度と短く、リアルタイムにがんの病勢を反映していることが示唆されています。従来、cfDNA測定の報告はdroplet digital PCR法や次世代シーケンサーによるものが主でしたが、私達は簡便に安価に繰り返し測定可能なリアルタイムPCR法によるcfDNA測定の可能性を検討しています。特に、抗がん剤の早期効果判定や測定可能病変のない消化器癌における増悪判定の代替マーカーとなるアッセイ系の確立を目指し、実地臨床への応用を期待しています。
背景:cfDNA fragmentと臨床的意義
臨床試験・治験一覧
食道癌
- ・一次治療:FP or FOLFOX+ペムブロリズマブ vs FP or FOLFOX+ペムブロリズマブ+レンバチニブ
- ・一次治療:FP+抗PD-1抗体+TAS-120:第1a/b相試験
- ・二次治療(ICI未治療):パクリタキセル+ペムブロリズマブ±抗LAG-3抗体:第1/2相試験
- ・二次治療以降(FGFR異常) フチバチニブ+ペムブロリズマブ:第1b相試験
胃癌
- ・一次治療(FGFR2b過剰発現)Bemarituzumab±FOLFOX:第3相試験
- ・一次治療(HER2陰性)CTx+Domvanalimab+Zimberelimab:第3相試験
- ・一次治療(HER2陽性)Chemo+Zanidatamab+Tisle:第3相試験
- ・二次治療(HER2陽性)DS-8201a vs ラムシルマブ+パクリタキセル:第3相試験
大腸癌
- ・一次治療(HER2陽性、OX未投与)Tucatinib+トラスツズマブ+FOLFOX/CAPOX±ペムブロリズマブ:第1/2相試験
- ・一次治療(BRAF V600E変異型)FOLFIRI ± セツキシマブ+エンコラフェニブ vs ± ベバシズマブ:第3相試験
- ・二次治療以降(TROP2陽性)Dato-Dxd:第2相試験
- ・三次治療以降(KRAS G12C変異型)AMG510+パニツムマブ+FOLFOX:第1相試験
- ・三次治療以降(KRAS G12C変異型)LY3537982+セツキシマブ:第1相試験
- ・三次治療以降ASP2074:第1相試験
固形癌
- ・標準治療抵抗(GPC3陽性:固形癌)ERY974:第1相試験
- ・ALK融合遺伝子陽性固形癌(非小細胞肺癌除く)ブリグチニブ:第2相試験
- ・EGFR遺伝子増幅陽性固形癌(食道・胃・小腸・尿路上皮)ネシツムマブ: 第2相試験(先進医療)
- ・その他FGFR3、METなどをターゲットとした治験があります